最新一期Science Bulletin(科学通报,影响因子11.780)期刊,以封面故事及两篇背靠背文章方式,发表了分别由两位中国临床专家纪立农教授和贾伟平教授牵头的西格列他钠与安慰剂对照、与西格列汀对照在2型糖尿病(T2DM)患者的确证性三期临床试验结果。该期刊同期还刊登了国际著名胰岛素抵抗研究和糖尿病临床专家、美国德州大学糖尿病中心主任DeFronzo教授就两项三期临床试验结果及意义的评论文章。
西格列他钠(Chiglitazar;国际通用名:Carfloglitazar)是一个全新PPAR全激动剂(PPAR-pan agonist),属微芯生物发现和全程自主研发,它能够平衡且不过度地同时激活与糖脂和能量代谢密切相关的PPARα、δ和γ三个受体亚型。前期综合研发结果显示,西格列他钠具有良好的人体药代动力学和药效动力学特征,并且在多项探索性临床试验中显示出对T2DM患者血糖和血脂具有综合调控作用,安全性良好。
这是全球首个PPAR全激动剂用于治疗T2DM的三期临床试验报道。两项三期研究结果表明,西格列他钠对生活方式控制血糖不佳的T2DM患者具有总体良好的疗效和安全性,为这一PPAR全激动剂治疗T2DM提供了确证性临床试验证据。DeFronzo教授的评论文章指出,西格列他钠在化学结构上与TZD类药物不同,在功能上它对PPAR三个受体亚型具有平衡的激动活性,在有效和持续控制血糖的同时,明确显示出了它在改善胰岛素抵抗和降低甘油三酯、游离脂肪酸的作用。DeFronzo教授还评论到,西格列他钠还显著降低谷草转氨酶和谷丙转氨酶,提示它在非酒精性脂肪性肝炎/非酒精性脂肪性肝病(NASH/NAFLD)治疗上的潜在前景。
西格列他钠是我国自主研发出的重磅原创性新药,是一次中国本土糖尿病新药从零到一的历史性突破,彰显了中国原创企业的创新精神与能力,也充分展现了中国专家在糖尿病临床研究中的科学严谨与能力。
以下为原刊于《科学通报》网站的报道:
2型糖尿病(T2DM)是糖尿病的主要类型,约占所有糖尿病总和的90%,是全球性重大疾病,目前在中国即有超过1亿患者。T2DM的核心发病机制为胰岛素抵抗及后继出现的胰岛功能失代偿,其重要特征为血糖、血脂和能量综合代谢紊乱,即患者除血糖升高外,还常常伴随血脂异常、高血压等代谢综合征症状。即使血糖得到控制,各种心血管事件的风险仍然显著高于非糖尿病患者,并成为T2DM患者死亡的最主要原因。T2DM作为一个慢性代谢性疾病,对人类的健康和生命造成严重威胁。
鉴于胰岛素抵抗是T2DM发生和发展中的重要病理机制,也是患者所伴随的代谢综合征及心血管疾病的重要原因,针对胰岛素抵抗的药物(胰岛素增敏剂)在临床应用中具有重要的地位和价值。既往已上市的噻唑烷二酮(TZD)类药物(包括罗格列酮和吡格列酮),是一类以核受体过氧化物酶体增生物受体γ(Peroxisome proliferator-activated receptor γ, PPARγ)为靶点的胰岛素增敏剂,它们在持续控制血糖上具有明确优势,同时也显示出降低心血管风险作用(如吡格列酮)。然而,与TZD类药物相关的一些安全性问题,如体重增加、水肿、充血性心力衰竭、骨折等副作用,也限制了这类药物在部分患者中的使用。
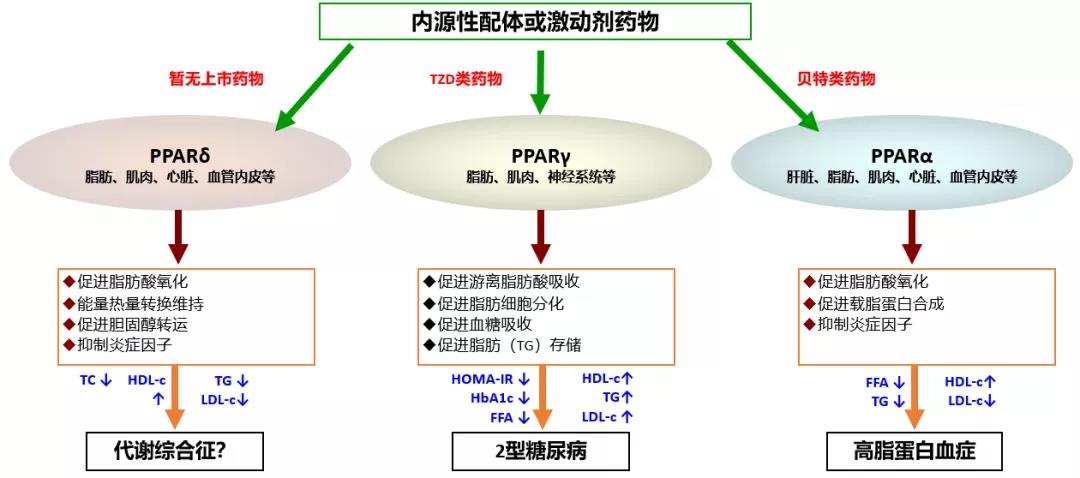
PPAR是体内调节糖脂和能量代谢的核受体家族,包括α、δ、γ三个亚型,它们在功能上既有重叠,也存在差异。PPARγ激动剂药物(TZD类药物)已经用于T2DM治疗,PPARα激动剂药物(贝特类)则用于高血脂治疗。虽然目前还没有针对PPARδ的药物用于临床,但已有研究表明它在脂代谢、体重和动脉粥样硬化的调控方面具有重要作用。据此,如果开发出一类化合物能够同时激活PPAR三个受体亚型,将有可能在T2DM治疗中实现控制血糖、血脂和能量代谢紊乱的综合作用;与此同时,鉴于三个PPAR亚型间具有相互拮抗的特点,PPARα和δ亚型的激活,有可能对抗PPARγ亚型激活所带来的潜在副作用,如体重增加和骨折。
西格列他钠(Chiglitazar Sodium;国际通用名Carfloglitazar)是由中国微芯生物公司自主研发的一个全新非TZD结构的PPAR全激动剂。前期综合研究结果显示,西格列他钠能够平衡且不过度激活PPARα、δ和γ三个受体亚型,具有良好的人体药代动力学特征,并且在多项探索性临床试验中显示出对T2DM患者血糖和血脂具有综合调控作用,安全性良好。
近日,Science Bulletin 杂志发表了分别由北京大学人民医院纪立农教授牵头的西格列他钠与安慰剂对照(CMAP)、上海交通大学附属第六人民医院贾伟平教授牵头的西格列他钠与西格列汀对照(CMAS)的两篇背靠背的确证性三期临床试验结果。
CMAP和CMAS均为多中心、随机、双盲、对照临床研究,分别入组了535和739例经饮食和运动不能有效控制血糖的T2DM患者,对比研究观察了西格列他钠32 mg和48 mg两个剂量分别与安慰剂(CMAP)或与已上市药物西格列汀100 mg(CMAS)在治疗24周后的综合疗效及安全性。两项三期临床试验综合结果表明,T2DM患者在分别经西格列他钠两个剂量治疗24周后,其糖化血红蛋白(HbA1c)绝对值较治疗前降低1.32%~1.52%,显示出两个剂量均具有持续和有临床意义的血糖控制作用。这一试验研究的主要疗效终点指标与安慰剂对比呈优效,与活性药西格列汀对比呈非劣效。在有效控制HbA1c同时,与西格列汀相比,西格列他钠两个剂量组,特别是48 mg剂量组,在空腹血糖、餐后2小时血糖、胰岛素抵抗指数、甘油三酯、游离脂肪酸等一系列次要疗效终点指标中,均显示出优于西格列汀的疗效趋势。安全性方面,西格列他钠两个剂量组与安慰剂和西格列汀对照组相比,在不良事件总体发生率和程度分级上均基本一致。两项试验中观察到西格列他钠治疗组出现较低频率的与PPARγ激活相关的副作用,如水肿事件和体重增加,但均明显低于TZD类药物的报道情况。
两项三期临床试验结果表明,西格列他钠对生活方式控制血糖不佳的T2DM患者具有总体良好的疗效和安全性,为这一PPAR全激动剂治疗T2DM提供了确证性临床试验证据。在全球范围内,这也是首个PPAR全激动剂在T2DM适应症上的三期临床试验报道。

同期还刊登了国际著名胰岛素抵抗研究和糖尿病临床专家、美国德州大学糖尿病中心主任DeFronzo教授就两项三期临床试验结果的评论文章——“Chiglitazar: a novel pan-PPAR agonist”。DeFronzo教授指出,PPARγ激动剂TZD类药物是强有力的胰岛素增敏剂,能够有效降低HbA1c,并在既往有心血管疾病史的糖尿病与非糖尿病患者中显示了心血管保护作用。然而,由于TZD药物的血管舒张效应和对肾脏PPARγ激活所导致的体内液体潴留,以及体重增加,限制了这类药物在T2DM患者上的治疗应用。根据PPAR不同亚型受体在体内组织分布及功能的不同,开发PPAR双激动剂(α/γ)和全激动剂(α/γ/δ)已是领域关注的趋势,其主要目的之一就是改善或预防TZD类药物的副作用。他进一步点评到,西格列他钠在化学结构上不是TZD类,在功能上它对PPAR三个受体亚型具有平衡的激动活性,而这样的活性在人体内能够被48 mg/天的剂量所覆盖。西格列他钠在有效和持续控制血糖的同时,明确显示出了它在改善胰岛素抵抗和降低甘油三酯、游离脂肪酸的作用。在安全性指标方面,DeFronzo教授评论到,西格列他钠显示了用药安全性,两个剂量下的不良事件发生率与安慰剂相当。大约有4.2%~4.8%服用西格列他钠的患者出现了水肿,但均为轻到中度;有1.1~1.9 kg的体重轻微增加。水肿事件和体重增加低于TZD类药物所报道的情况,但后续需要通过头对头的对比研究才能得出明确的结论。此外,西格列他钠还显著降低谷草转氨酶和谷丙转氨酶,提示它在非酒精性脂肪性肝炎/非酒精性脂肪性肝病(NASH/NAFLD)治疗上的潜在前景。
转自:微芯生物
